|
||||
|
ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА И МАГИСТРАЛЬНЫХ СОСУДОВ КлассификацияКлассификация врожденных пороков сердца должна основываться на характере анатомических нарушений, а также учитывать степень гемодинамических расстройств и оценку клинического статуса. Аномалии развития сердца и магистральных сосудов сопровождаются различными нарушениями гемодинамики, которые подразделяют на первичные, возникающие сразу же после рождения ребенка, и вторичные, являющиеся следствием течения врожденного порока сердца. Первичные нарушения гемодинамики I. Гиперволемия малого круга кровообращения с перегрузкой: а) правого желудочка (дефект межпредсердной перегородки, аномальный дренаж легочных вен); б) левого желудочка (открытый артериальный проток, дефект аортолегочной перегородки); в) обоих желудочков (дефект межжелудочковой перегородки, транспозиция магистральных сосудов). II. Затруднение выброса крови из: а) правого желудочка (различные формы сужения выводного тракта правого желудочка и легочной артерии); б) левого желудочка (различные формы сужения выводного тракта левого желудочка и аорты). III. Затруднение в наполнении желудочков кровью: а) правого (сужение правого атриовентрикулярного отверстия); б) левого (врожденное сужение левого атриовентрикулярного отверстия). IV. Объемная перегрузка желудочков сердца вследствие врожденной клапанной недостаточности: а) правого (недостаточность трехстворчатого клапана и клапана легочной артерии); б) левого (недостаточность митрального клапана и клапана аорты). V. Гиповолемия малого круга кровообращения с одновременным увеличением минутного объема в большом круге кровообращения, обусловленная ранним сбросом венозной крови в большой круг кровообращения (тетрада Фалло, триада Фалло, некоторые формы транспозиции магистральных сосудов и т. д.). VI. Смешение венозной крови с артериальной при отсутствии гемодинамически значимого сброса крови из одного круга кровообращения в другой (общее предсердие, некоторые формы транспозиции магистральных сосудов). VII. Выброс всей венозной крови в большой круг кровообращения с экстракардиальными механизмами компенсации (общий артериальный ствол). Вторичные нарушения гемодинамики Они возникают вследствие развития вторичных анатомических процессов в сосудах малого круга кровообращения или в миокарде. I. Увеличение минутного объема крови большого круга кровообращения вследствие возникшего сброса венозной крови в артериальную через легочные артериовенозные и артериоартериальные шунты. Эти нарушения гемодинамики наблюдаются при развитии резко выраженного склероза сосудов малого круга кровообращения (вторичной легочной гипертонии) при дефектах перегородок сердца, открытом артериальном протоке, дефекте в перегородке между аортой и легочной артерией. II. Различные формы декомпенсации сердечной деятельности. III. Артериальная гипертония в сосудах верхней половины тела и гипотония в нижних при коарктации аорты. Классификация врожденных пороков сердца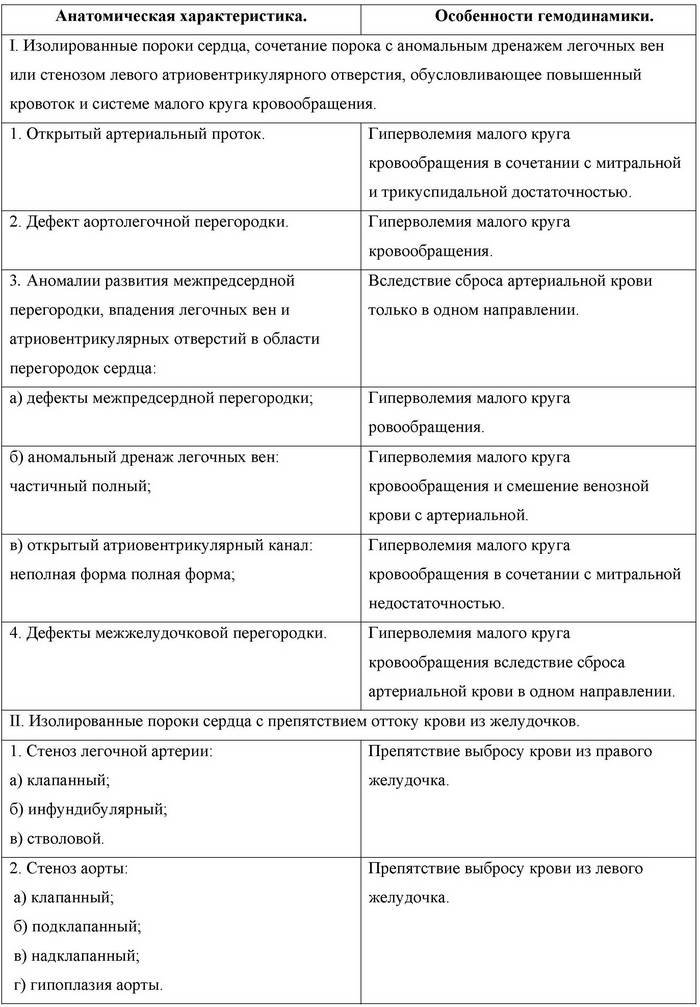   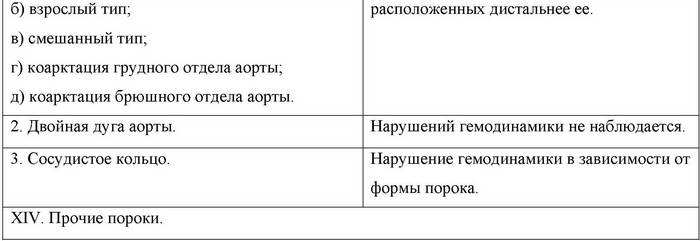 Основные патофизиологические и морфологические изменения в организме вследствие нарушений кровообращения у больного врожденным пороком сердца. Врожденный порок сердца вызывает у больного в первую очередь функциональные сдвиги компенсаторного порядка. Хроническая гипоксемия и нарушение кровообращения ведут к компенсаторной перестройке всех систем организма. Однако процессы компенсации у ряда больных перерастают в свою противоположность, обусловливая преждевременную гибель организма. Снижение насыщения артериальной крови кислородом (артериальная гипоксемия) у больных врожденными пороками сердца обычно наблюдается при поступлении (сбросе) венозной крови в артериальную. Лишь в поздних стадиях заболевания при тяжелой декомпенсации сердечной деятельности и выраженном склерозе сосудов легких артериальная гипоксемия может быть обусловлена недостаточным насыщением крови кислородом в легочных капиллярах. Артериальная гипоксемия вследствие сброса венозной крови в артериальную наблюдается при различных анатомических изменениях. Все компенсаторные механизмы у больного, страдающего хронической гипоксемией, направлены на улучшение (облегчение) доставки тканям кислорода. Это проявляется в увеличении содержания гемоглобина и эритроцитов (полиглобулия и нодицитемия), причем у некоторых больных с тяжелой артериальной гипоксемией содержание гемоглобина может быть выше 100 г/л, а число эритроцитов более 10* 109 /л. Наряду с этим у больных смещается кривая диссоциации гемоглобина, Увеличивается объем циркулирующей крови в головном мозге. Это может приводить к развитию отека мозга и возникновению кровоизлияний при малейших расстройствах дыхания и кровообращения. Определенные изменения, связанные с хронической гипоксемией, наблюдаются и в веществе головного мозга. При выраженной хронической гипоксемии в головном мозге развиваются глубокие патоморфологические сдвиги. Эти сдвиги, первоначально носящие компенсаторный характер, постепенно обусловливают развитие тяжелого патологического фона. Последний резко затрудняет проблему хирургического лечения таких больных. В связи с уменьшением минутного объема крови в системе малого круга кровообращения при сбросе венозной крови в артериальную в легких также развиваются патоморфологические сдвиги, направленные в первую очередь на повышение эффективности вентиляции и развитие коллатерального кровообращения между сосудами малого и большого круга кровообращения. Миокард больных врожденными пороками сердца находится в состоянии компенсаторной гиперфункции. В зависимости от характера и выраженности нарушений гемодинамики преобладает тоногенная дилатация или гипертрофия миокарда. У многих больных непрерывная нагрузка на миокард и патологические сдвиги биохимических, обменных и энергетических процессов в сердечной мышце сопровождаются развитием морфологических изменений в миокарде, что приводит к возникновению сердечной недостаточности. Степень гипертрофии миокарда при различных врожденных пороках сердца неодинакова – она больше при пороках, сопровождающихся препятствием к выбросу крови из желудочков, и меньше при изолированных дефектах межпредсердной и межжелудочковой перегородок, а также при незаращении артериального протока. Самая высокая степень гипертрофии миокарда развивается при врожденных пороках сердца с наличием значительных сужений на пути тока крови. Увеличение количества интрамуральных сосудистых ветвей в гипертрофированных отделах миокарда не является специфической особенностью врожденных пороков сердца, однако оно выражено в большей степени, чем при гипертрофии сердца другой этиологии. Это отличие миокарда при врожденных пороках сердца объясняется: 1) наличием стимула для новообразования сосудов, действующего со дня рождения – гипоксии миокарда; 2) незакончившейся дифференцировкой миокарда к тому моменту, когда начинает действовать стимулирующее влияние гипоксии. У ряда больных наблюдается развитие кардиосклероза, наиболее выраженного в тех отделах сердца, которые находились в состоянии компенсаторной гиперфункции, а затем гипертрофии. Кардиосклероз, как правило, более выражен во внутренних слоях, в трабекулярных и папиллярных мышцах, где располагаются наиболее гипертрофированные сердечные мышечные волокна. Легочная гипертония может быть следствием ряда заболеваний сердечно-сосудистой системы или является самостоятельным заболеванием. От соотношения величин легочного сосудистого сопротивления и легочного кровотока зависит давление в малом круге кровообращения. Институте сердечно-сосудистой хирургии им. А. Н. Бакулева АМН СССР разработана классификация легочной гипертонии с учетом всех параметров гемодинамики в малом круге кровообращения и их отношения к таковым в большом круге кровообращения (Бураковский В. И. И соавт., 1975). Согласно этой классификации, выделяются четыре группы легочной гипертонии; В первых трех группах при различных величинах давления и общего легочного сосудистого сопротивления существует сброс крови слева направо, а в четвертой группе он имеет обратное направление. Сопоставление нарушений гемодинамики в пределах учитываемых в классификации параметров с морфологией сосудистой системы легких показало, что гипертония во второй и третьей А группах в основном носит функциональный характер, в третьей Б группе морфологические изменения настолько выражены, что после коррекции порока давление в легочной артерии не снижается до нормального уровня и, следовательно, в патогенезе гипертонии превалирует органический компонент. В четвертой группе гипертония в легочной артерии целиком обусловлена изменениями структуры легочных сосудов и носит необратимый характер. Выделяют 3 основных типа легочной гипертонии: 1) пассивная – развивающаяся вследствие высокого венозного давления при левожелудочковой недостаточности, миксоме левого предсердия и т. п.; 2) гиперкинетическая – за счет артериовенозных анастомозов, развитие своеобразных структур типа клубков и ангиомоподобных сосудов; 3) обтурационная, возникающая при закупорке легочных сосудов, в том числе: а) обструкционная – при блокаде кровотока с внешней стороны легочных сосудов; б) облитеративная – при структурных изменениях в стенке легочных сосудов; в) вазоконстриктивная – при функциональном спазме сосудов мышечного типа; г) многофакторная. При некоторых врожденных пороках сердца большой объем сброса крови слева направо сопровождается значительной перегрузкой малого круга кровообращения, которая приводит к резкому растяжению и расширению легочных сосудов. При длительно существующем спазме мелких артерий и артериол развивающиеся органические изменения носят двоякий характер: 1) компенсаторно-приспособительный; 2) патологический. К изменениям компенсаторно-приспособительного характера относятся перекалибровка сосудов, перестройка артериол по типу мелких артерий, расширение капиллярной сети, увеличение ее за счет включения резервных капилляров, гиперэластоз артерий эластичного типа, гипертрофия мышечной оболочки артерий мышечного типа, увеличение числа артериоартериальных и артериовенозных анастомозов, развитие своеобразных структур типа клубков и ангиомоподобных сосудов. Патологический характер изменений заключается в атеросклерозе легочной артерии, расширении ствола и крупных ветвей ее, интимальном фиброэластозе с сужением просвета сосудов, плазматическом пропитывании, гиалинозе и фиброзе стенки мелких артерий. Классификация легочной гипертонии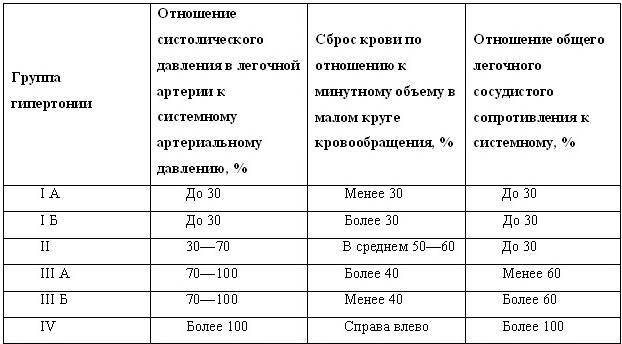 При длительно существующей гиперволемии и гипертонии обнаруживаются изменения в легочной ткани и бронхах, которые выражаются в неравномерном утолщении межальвеолярных перегородок, скоплении бурого пигмента, наличии мелких очагов ателектаза и эмфиземы. Таким образом, при врожденных пороках сердца в организме развивается сложная система новых качественных взаимосвязей биохимического, патофизиологического и патоморфологического порядка. Все эти сдвиги связаны с включением компенсаторно-приспособительных механизмов в ответ на нарушения кровообращения. Такое состояние организма характеризуется, во-первых, использованием в определенной степени его резервных возможностей, (т. е. непрерывным напряжением механизмов компенсации), во-вторых, развитием цепи вторичных патологических сдвигов, рано или поздно обусловливающих состояние декомпенсации. ОТКРЫТЫЙ АРТЕРИАЛЬНЫЙ (БОТАЛЛОВ) ПРОТОК Артериальный проток – сосуд, соединяющий аорту с легочной артерией, – играет важную роль в кровообращении плода. После рождения ребенка проток обычно облитерируется и превращается в артериальную связку. Незаращение протока ведет к образованию порока сердца. Порок наблюдается в среднем у 20 % всех детей с врожденными пороками сердца. Открытый артериальный проток может быть самостоятельным заболеванием или сочетаться с другими врожденными пороками сердца. Анатомия, гемодинамикаАртериальный проток располагается в верхнем отделе переднего средостения и прикрыт листком париетальной плевры. Проток отходит от аорты на уровень отхождения левой подключичной артерии и в большинстве случаев соединяется со стволом легочной артерии в месте деления последнего на правую и левую легочные артерии. Диаметр протока обычно не превышает 1–1,5 см. При открытом артериальном протоке артериальная кровь благодаря разнице в давлении поступает из аорты в легочную артерию. Поступление дополнительного количества крови из аорты в малый круг кровообращения ведет к перегрузке сосудов легких, левого предсердия и левого желудочка. По мере повышения сопротивления в сосудах легких в них возникает склеротический процесс и нарастает легочная гипертония. Клиническая картинаОбщие проявления порока мало характерны. Дети, как правило, физически хорошо развиты, нормально упитаны, однако некоторые все-таки отстают в развитии, быстро устают. При большом диаметре открытого артериального протока по мере роста ребенка и развития легочной гипертонии больные постепенно начинают предъявлять жалобы. У маленьких детей с большим сбросом крови наблюдаются симптомы плохо купирующейся недостаточности кровообращения, частые пневмонии, одышка. При аускультации больного с открытым артериальным протоком слышен характерный непрерывный систолодиастолический шум с максимальным звучанием во II межреберье слева от грудины. В литературе этот шум обозначают как «шум мельничного колеса», «шум грохота поезда в тоннеле» или «машинный шум». При глубоком вдохе интенсивность шума ослабевает, а во время выдоха и задержки дыхания усиливается. У детей в возрасте до 2 лет интенсивность шума значительно слабее. Определяется акцент II тона над легочной артерией. Выявляется несколько повышенный уровень систолического АД; диастолическое АД резко снижено (иногда до нуля). При развитии тяжелой легочной гипертонии (IIIБ группы) шум исчезает, так как общее легочное сосудистое сопротивление достигает величины системного и сброс крови прекращается. На ФКГ, снятой во II межреберье слева от грудины, удается фиксировать непрерывный систолодиастолический шум и увеличение амплитуды II тона. На ЭКГ при значительном сбросе крови регистрируются признаки перегрузки левого желудочка. При нарастании легочной гипертонии выявляются симптомы перегрузки правых отделов сердца. У детей раннего возраста на ЭКГ отмечается перегрузка обоих желудочков сердца. При рентгенологическом исследовании определяется усиление легочного рисунка за счет перенапряжения артериального русла, увеличение левого желудочка, а в косых проекциях – и левого предсердия, выбухание дуги легочной артерии. При рентгеноскопии видна усиленная пульсация восходящей аорты. Диагноз, как правило, можно безошибочно поставить, не прибегая к зондированию сердца. Двухмерная эхокардиография позволяет увидеть проток в области бифуркации легочного ствола и оценить его ширину. Допплер-эхокардиография обнаруживает патологический диастолический поток крови в легочном стволе и в нисходящей аорте на уровне отхождения протока. При катетеризации сердца обнаруживается повышение насыщения крови кислородом на уровне легочной артерии. У больных с гипертонией малого круга кровообращения регистрируется повышенное давление в системе легочной артерии и в правом желудочке. При ангиокардиографическом исследовании методом выбора является аортография, которая позволяет видеть сброс контрастированной крови из аорты в легочную артерию. Иногда можно увидеть сам проток и точно судить о его ширине. Осложнениями этого порока являются развитие легочной гипертонии и возникновение бактериального эндокардита. ЛечениеНеобходимо хирургическое вмешательство. Операция, как правило, заключается в перевязке открытого артериального протока. Некоторые хирурги предлагают перевязывать открытый артериальный проток, а затем накладывать непрерывный шов как со стороны аорты, так и со стороны легочной артерии. Отдаленные результаты очень хорошие. ДЕФЕКТ МЕЖПРЕДСЕРДНОЙ ПЕРЕГОРОДКИ (ДМПП) Порок встречается у 8—16 % больных с врожденными пороками сердца, чаще у лиц женского пола. Анатомия, классификация, гемодинамикаВ зависимости от расположения дефекта и эмбриологических особенностей развития перегородки различают: 1) дефект первичной перегородки – тип ostium primum; 2) дефект вторичной перегородки – тип ostium secundum. Дефект первичной межпредсердной перегородки всегда расположен в определенном месте – над атриовентрикулярными клапанами и сочетается у превалирующего большинства больных с патологией атриовентрикулярпых клапанов. Дефект вторичной межпредсердной перегородки может быть расположен: а) в центральном отделе перегородки; б) в задненижнем отделе у устья нижней полой вены; в) в верхнем отделе (так называемый высокий дефект), у устья верхней полой вены. Дефекты вторичной перегородки могут быть множественными, когда перегородка является фенестрированной, и комбинированными, когда сочетаются различные типы дефектов. При дефектах межпредсердной перегородки наблюдается сброс крови из левого предсердия в правое. Это ведет к повышению минутного объема в малом круге кровообращения и увеличению нагрузки на правый желудочек. Давление в легочной артерии при дефекте межпредсердной перегородки возрастает только в поздних стадиях заболевания, при развитии склероза сосудов малого круга кровообращения. Как правило, порок характеризуется невысоким общим сопротивлением легочных сосудов, тогда как артериовенозный сброс крови может достигать значительных величин. Клиническая картинаКлинические проявления порока разнообразны, иногда бывают выражены слабо. Основной жалобой больных является одышка при физической нагрузке. Кожные покровы бледны. При тяжелом течении в раннем возрасте могут наблюдаться симптомы недостаточности кровообращения. При аускультации больного с межпредсердным дефектом определяется систолический шум с максимальной точкой звучания во II–III межреберье слева от грудины. Шум умеренный, отличающийся от грубого систолического шума при дефекте межжелудочковой перегородки. Тембр и интенсивность шума могут быть различными, причем интенсивность возрастает при задержке дыхания на выдохе. У некоторых больных шум короткий, скребущего характера. Над местом проекции клапана легочной артерии у большинства больных регистрируется акцент II тона. На фонограмме, записанной во II–III межреберье слева от грудины, фиксируется систолический шум невысокой амплитуды, оканчивающийся усиленным II тоном. Электрокардиографическое исследование позволяет выявить весьма характерные признаки порока: наряду с гипертрофией правого желудочка определяются выраженные признаки перегрузки его вследствие гиперволемии. У 65 % больных наблюдается блокада правой ножки пучка Гиса. Рентгенологическое исследование имеет весьма существенное значение в диагностике изолированного дефекта межпредсердной перегородки. Легочный рисунок усилен (за счет переполнения артериального русла) тем значительнее, чем больше объем сброса крови. Сердце увеличено в поперечнике, выбухает дуга легочной артерии. В косых проекциях определяется увеличение правых отделов сердца. Аорта при этом гипопластична, слабо пульсирует, тогда как амплитуда пульсации легочной артерии увеличена. Характерным признаком дефекта межпредсердной перегородки, определяемым при рентгеноскопии, является пульсация корней легких. Катетеризация сердца дает возможность выявить сброс крови на уровне предсердий, определить его объем, провести катетер из правого предсердия в левое, а также измерить давление в правом желудочке и легочной артерии. Желательно выполнять ангиокардиографию с селективным введением контрастного вещества в легочную артерию. При эхокардиографическом исследовании в случаях вторичного дефекта межпредсердной перегородки обнаруживается перерыв эхосигнала от межпредсердной перегородки (для верификации диагноза подобный перерыв эхосигнала должен быть зафиксирован не менее чем в 2–3 проекциях), в сочетании с признаками объемной диастолической перегрузки правых отделов сердца. Учитывая особенности гемодинамики и объемную перегрузку правого желудочка и малого круга крвообращения, а также позднее развитие легочной гипертонии, которая бывает обусловлена склеротическими изменениями сосудов легких, по клиническому течению и по нарушению гемодинамики можно выделить 5 групп больных с дефектом межпредсердной перегородки: 1) у больных первой группы дефект межпредсердной перегородки не сопровождается определенной клинической симптоматикой. Они чувствуют себя хорошо, не предъявляют жалоб и лишь при аускультации обнаруживается систоличекий шум во II–III межреберье у левого края грудины, что служит единственным симптомом врожденного порока сердца. ЭКГ и рентгенологические размеры сердца у этих больных обычно в пределах нормы; 2) у больных второй группы выявляется достаточно четкая картина дефекта межпредсердной перегородки, значительно увеличены правые отделы сердца, расширен ствол легочной артерии. На ЭКГ регистрируется правограмма, однако давление в легочной артерии и правом желудочке не превышает 30 мм рт. ст.; 3) у больных третьей группы уже выявляются симптомы легочной гипертонии, возникающей вследствие склероза сосудов малого круга кровообращения. У этих больных наблюдается значительный сброс крови из левого предсердия в правое и резко расширены границы сердца; 4) четвертую группу составляют тяжелобольные, клиническая картина болезни которых осложняется появлением тяжелых нарушений сердечного ритма с симптомами недостаточности кровообращения; 5) больные пятой группы страдают выраженной легочной гипертонией с обратным сбросом крови через дефект, что обусловливает развитие цианоза. Эти больные безнадежны, и лишь успешная трансплантация сердца и легких может продлить им жизнь. ЛечениеТолько оперативное. Производится ушивание или пластика заплатой дефекта межпредсердной перегородки в условиях искусственного кровообращения. Непосредственные и отдаленные результаты хирургического вмешательства очень хорошие. Смертность после операции минимальна, а плохие результаты могут быть лишь у больных с тяжелой формой легочной гипертонии. ДЕФЕКТ МЕЖЖЕЛУДОЧКОВОЙ ПЕРЕГОРОДКИ Порок встречается достаточно часто, по данным разных авторов, он выявляется в 15–25 % случаев всех врожденных пороков сердца. Анатомия, гемодинамикаВажное значение для клинического течения имеют большие дефекты межжелудочковой перегородки, располагающиеся ниже наджелудочкового гребня. Различают также дефекты, располагающиеся в самых различных отделах мышечной части межжелудочковой перегородки. Еще одна группа дефектов – это дефекты, располагающиеся выше наджелудочкового гребня под клапаном легочной артерии у корня аорты. Эти дефекты часто сопровождаются недостаточностью аортального клапана. Очень распространены дефекты, располагающиеся ниже наджелудочкового гребня и в области комиссур трикуспидального клапана, так называемые комиссуральные дефекты (сравнительно небольших размеров, с фиброзными краями). В последние годы в ведущих клиниках мира используется классификация межжелудочковых дефектов, предложенная В. Soto и соавт. (1980). Согласно этой классификации дефекты подразделяются на приточные, трабекулярные и выводные в зависимости от локализации в соответствующем отделе перегородки. Кроме того, учитывается отношение дефектов к мембранозной перегородке и магистральным сосудам, в результате чего они делятся на перимембранозные, субартериальные и не связанные с этими структурами мышечные дефекты. При изучении гемодинамики выделяют 2 группы больных с дефектами межжелудочковой перегородки. Больные первой группы имеют большой дефект межжелудочковой перегородки. Уже в течение первого года после рождения у них наблюдается большой объем сброса крови из левого желудочка в правый, переполнение малого круга кровообращения и гиперкинетическая форма легочной гипертонии. Наличие большого сброса крови и повышение давления в системе легочной артерии ведет к перегрузке левого и правого желудочков, которая обусловливает развитие выраженной декомпенсации кровообращения. У этих больных очень рано наблюдается наступление структурных изменений в легких и развитие вторичной легочной гипертонии. У больных второй группы (размеры дефекта составляют 0,5–1,5 см) нарушение гемодинамики более умеренное; наблюдается небольшой сброс крови через дефект и возрастание легочного кровотока, однако легочная гипертония развивается только в более позднем возрасте, а сердечной недостаточности, как правило, не наблюдается. Клиническая картинаОна бывает обусловлена сбросом крови через дефект, степенью легочной гипертонии, наличием той или иной формы сердечной недостаточности. Дети с большими дефектами межжелудочковой перегородки часто отстают в физическом развитии. У некоторых из них наблюдается сердечный горб. Раннее появление сердечной недостаточности ведет к выраженной бледности кожных покровов, малой подвижности детей. Дети с большими дефектами межжелудочковой перегородки, недостаточностью кровообращения долгие месяцы находятся на госпитальном лечении. Однако при сравнительно небольших дефектах межжелудочковой перегородки дети хорошо растут и развиваются. Для дефектов межжелудочковой перегородки характерен грубый систолический шум, интенсивность и распространение которого в значительной степени зависят от величины дефекта и степени и развития легочной гипертонии. У больных первой группы (с небольшим дефектом и умеренным сбросом крови) над сердцем выслушивается грубый систолический шум. Легко найти точку максимального звучания шума, так как он обусловлен сравнительно узкой струей крови, бьющей из левого желудочка в правый через дефект в перегородке. У больных с легочной гипертонией второй группы выслушивается над сердцем разлитой, очень грубый шум, который проводится на легочную артерию и далеко на сосуды; определяется также резко выраженный акцентированный II тон над легочной артерией. У больных третьей группы интенсивность шума зависит от величины сброса крови. Постепенно по мере развития легочной гипертонии интенсивность шума уменьшается; у больных четвертой группы шум исчезает вследствие прекращения сброса крови через дефект. У этих больных определяется очень характерная аускультативная картина – короткий сухой систолический шум незначительной интенсивности и резко выраженный (с металлическим звучанием) щелчок захлопывания клапана легочной артерии. У некоторых больных выслушивается диастолический шум Грехема—Стилла. Электрокардиографические изменения у больных первой группы мало выражены – отмечаются лишь признаки небольшой перегрузки левых отделов сердца. У больных второй группы выявляются характерные изменения ЭКГ: из-за резко выраженного сброса крови через дефект и повышения давления в легочной артерии развиваются признаки перегрузки обоих желудочков. Приблизительно в половине случаев наблюдается отклонение электрической оси сердца влево. У больных третьей группы при постепенном нарастании давления в легочной артерии происходит смещение электрической оси сердца вправо. У всех больных четвертой группы резко выражена правограмма. Рентгенологические данные находятся в прямой зависимости от степени расстройств гемодинамики. У больных первой группы сердце умеренно увеличено в размерах, обычно несколько увеличен левый желудочек, легочный рисунок умеренно усилен. У больных второй и третьей групп сердце расширено в поперечнике, больше увеличен левый желудочек, резко выражено усиление легочного рисунка. У больных четвертой группы рентгенологическая картина весьма характерна – вследствие развившейся легочной гипертонии, исчезновения сброса крови через дефект и резко выраженной гипертрофии правого желудочка с элементами гипертрофии левого желудочка, размеры сердца увеличены (однако в значительно меньшей степени, чем у больных второй группы); корни легких расширены, имеются признаки застоя, видны резко расширенный ствол и прикорневые разветвления легочной артерии. В то же время на периферии легочный рисунок кажется обедненным – резко выраженный склероз сосудов легких приводит к уменьшению наполнения сосудистого русла. Двухмерная эхокардиография при дефекте межжелудочковой перегородки позволяет выявить прямой признак дефекта – перерыв эхосигнала от перегородки; установить количество дефектов, локализовать место дефекта по отношению к атриовентрикулярным и полулунным клапанам и определить его размеры. Допплер-эхокардиография выявляет турбулентный поток крови через дефект. У больных с изолированным дефектом межжелудочковой перегородки при расчете объема потока крови в легочной артерии и аорте возможно определить объем артериовенозного сброса. Зондирование сердца у больных с дефектами межжелудочковой перегородки следует выполнять по строго разработанной программе. Зондирование правых отделов сердца и легочной артерии позволяет исследовать кровь на насыщение ее кислородом, а также определить давление в легочной артерии, правом желудочке и правом предсердии. Затем в обязательном порядке больному следует сделать вентрикулографию. Съемку следует производить в двух проекциях. У больных с легочной гипертонией, особенно у детей раннего возраста, необходимо произвести аортографию. Зондирование сердца дает возможность получить полное представление о нарушениях гемодинамики, а вентрикулография позволяет выявить уровень расположения дефекта, исключить возможное наличие множественных дефектов. У больных с легочной гипертонией аортография позволяет исключить наличие сопутствующего открытого артериального протока. Данные зондирования сердца в сочетании с изучением клинико-рентгенологической картины и данных ЭКГ позволяют отнести больного к той или иной гемодинамической группе по величине легочной гипертонии. ЛечениеБольных, относящихся к 1-й группе, оперировать не следует. Все больные 2-й и 3-й групп подлежат безотлагательной операции. Больным 4-й группы операция противопоказана. Особое место в определении показаний к операции представляет собой группа детей в возрасте до 1 года. Многие авторы склоняются к мнению, что необходимо первичное закрытие дефекта межжелудочковой перегородки в условиях искусственного кровообращения (в сочетании с кардиоплегией или применением глубокой гипотермии). Однако тяжелобольным в возрасте до 3–4 месяцев, особенно если дефект сочетается с открытым артериальным протоком или коарктацией аорты, целесообразно выполнять паллиативную операцию сужения легочной артерии. При своевременном закрытии дефекта отдаленные результаты очень хорошие, при наличии тяжелой легочной гипертонии они зависят от выраженности структурных изменений в легочных сосудах. У некоторых больных при тяжелых формах легочной гипертонии давление в легочной артерии продолжает оставаться высоким, а в ряде случаев даже нарастает. КОАРКТАЦИЯ АОРТЫ Коарктация аорты встречается у 15 % больных с врожденными пороками сердца, причем в несколько раз чаще у мужчин, чем у женщин. Анатомия, классификация, гемодинамикаПорок представляет собой сужение или полный перерыв в области перешейка аорты, на границе дуги и нисходящего отдела аорты. Левая подключичная аортерия в 90 % случаев отходит от престенотического участка аорты, в 4–6 % – непосредственно в месте сужения, в 3–4 % – от постстенотического участка. В классификации, разработанной в Институте сердечно-сосудистой хирургии им. А. Н. Бакулева РАМН выделены 3 типа порока: 1) изолированная коарктация аорты; 2) коарктация аорты в сочетании с открытым артериальным протоком; 3) коарктация аорты в сочетании с другими врожденными пороками сердца (этот тип встречается в 10 % случаев). При взрослом типе порока (с заращенным артериальным протоком) механическое препятствие на пути кровотока в аорте вест к развитию двух режимов кровообращения. Проксимальнее сужения АД повышено, что сопровождается увеличением минутного объема и работы левого желудочка. Дистальнее препятствия АД (особенно пульсовое) снижено, кровоснабжение частично, а иногда и полностью осуществляется за счет коллатералей. Снижение пульсового АД ведет к включению почечного механизма развития вторичной нейроэндокринной гипертонии. При «инфантильном» типе с открытым артериальным протоком в зависимости от локализации различают предуктальную и постдуктальную коарктацию аорты. Предуктальный вариант коарктации в большинстве случаев характеризуется веноартериальным сбросом крови (через проток из легочной артерии в аорту), в результате чего резко увеличивается работа правого желудочка. Для постдуктального варианта характерен артериовенозный сброс крови через открытый артериальный проток. Таким образом, оба варианта этого типа коарктации аорты ведут к нарушению легочного кровообращения. Клиническая картинаБольные коарктацией аорты обычно жалуются на головные боли, носовые кровотечения, одышку, похолодание нижних конечностей. При осмотре у больных старше 10 лет отмечается хорошее развитие грудной клетки, плечевого пояса, шеи при отставании в развитии нижних конечностей. АД на руках повышено, на ногах снижено или вообще не определяется. В старшем возрасте могут пальпаторно определяться пульсация межреберных артерий, усиление верхушечного толчка, нередко пальпируется систолическое дрожание во II–III межреберье. Аускультативно определяется систолический шум над всей поверхностью сердца, проводящийся на сосуды шеи и в межлопаточное пространство; II тон над аортой акцентирован. В раннем детском возрасте может наблюдаться цианоз, преимущественно на ногах, в большинстве таких случаев выражены симптомы сердечной недостаточности. В заключительной стадии заболевания возможны осложнения: 1) кровоизлияние в мозг; 2) сердечная недостаточность; 3) образование и разрыв аневризмы аорты и межреберных артерий; 4) эндокардит; 5) и кальциноз аорты. Объемная сфигмография позволяет зарегистрировать увеличение объемного кровотока и повышение АД на верхних конечностях и снижение этих показателей на нижних конечностях. На ЭКГ выявляются различные изменения: от правограммы у детей до левограммы у взрослых с признаками гипертрофии левого желудочка и недостаточности коронарного кровообращения. На рентгенограммах в переднезадней проекции у 70–80 % больных определяется узурация ребер, возникающая от давления расширенных межреберных артерий. Конфигурация сердца близка к аортальной, тень восходящей аорты расширена, дуга аорты часто не дифференцируется. В левом переднем косом положении наряду с признаками увеличения левого желудочка при контрастировании пищевода видны два вдавления в виде цифры «3» за счет расширения аорты выше и ниже сужения. При двухмерной эхокардиографии визуализируются место сужения аорты, его диаметр и протяженность, а также соотношения с ветвями дуги аорты и открытым артериальным протоком. С помощью допплер-эхокардиографии можно определить систолический турбулентный кровоток и градиент давления в месте коарктации. Характерным признаком, выявляемым при катетеризации сердца, служит градиент систолического давления между восходящей и нисходящей аортой. При предуктальном варианте катетер из легочной артерии легко проходит через открытый артериальный проток в нисходящую аорту, где определяется снижение насыщения крови кислородом. Ангиокардиография показана в тех случаях, когда необходимо уточнить анатомические детали порока и диагностировать сопутствующие пороки. Методом выбора является аортография. Прогноз зависит от формы и своевременности обнаружения порока; многие больные раньше погибали в раннем возрасте от сердечной недостаточности. ЛечениеУ новорожденных и детей раннего возраста порок может привести к развитию декомпенсации кровообращения, что требует выполнения неотложной операции. В последнее время у таких больных с успехом стали применять баллонную дилатацию коарктации. При благоприятном течении порока оптимальным для операции является возраст 8—14 лет. В настоящее время применяются следующие методы устранения коарктации аорты: 1) резекция с анастомозом конец в конец; 2) резекция с протезированием аорты; 3) прямая и непрямая истмопластика; 4) шунтирование. Из осложнений следует отметить артериальную гипотонию, которая может развиться сразу после восстановления тока крови по аорте, а также парадоксальную артериальную гипертонию, абдоминальный синдром и кровотечение, развивающиеся в ближайшем послеоперационное периоде. Послеоперационная летальности при неосложненных формах порока у детей (10–15 лет колеблется от 0,5 до 6 %, у грудных детей при наличии сердечной недостаточности она достигает 25 %. ТЕТРАДА ФАЛЛО Тетрада Фалло – один из тяжелейших и наиболее распространенных врожденных пороков, встречающийся в 12–14 % случаев всех врожденных пороков сердца. АнатомияОснову порока составляют нарушения развития выводного тракта правого желудочка и легочной артерии, большой дефект межжелудочковой перегородки, декстропозиция аорты, а также резко выраженная гипертрофия мышцы правого желудочка. Препятствие оттоку крови из правого желудочка может быть обусловлено стенозом инфундибулярного отверстия, сужением клапанного кольца легочной артерии и самого легочного ствола. Подклапанный стеноз, образующийся в результате недоразвития выходного отдела правого желудочка, как правило, резко выражен. У большинства больных он сочетается с нарушением развития клапанного кольца, которое сужено, а створки клапана зачастую сращены. Часто встречается двухстворчатый клапан легочной артерии. Легочный ствол у большинства больных уже, чем в норме. Степень сужения клапанного отверстия легочного ствола может быть различной, вплоть до атрезии устья легочной артерии или атрезии всего ее ствола. Степень декстропозиции аорты у больного с тетрадой Фалло также сильно колеблется. Расположение дефекта межжелудочковой перегородки при тетраде Фалло всегда постоянно – ниже аортального клапана. Его верхний край образован фиброзным кольцом аортального клапана, левый и нижний края – вначале левой ножкой наджелудочкового гребня, затем мышечной частью межжелудочковой перегородки, правый – перегородочной створкой трикуспидального клапана. На основании исследований, проведенных в Институте сердечно-сосудистой хирургии им. А. Н. Бакулева РАМН выделено 4 анатомические формы порока. 1. Эмбриологический тип обструкции выводного отдела правого желудочка, обусловленный смещением влево, а также в ряде случаев низким внедрением конусной перегородки. Максимальное сужение выводного отдела локализовано в основном на уровне разграничительного мышечного кольца. Кольцо легочного клапана обычно нормально развито либо несколько гипоплазировано. 2. Гипертрофический тип обструкции выводного отдела, вызванный смещением влево, а также резко выраженной гипертрофией проксимального сегмента конусной перегородки. Максимальное сужение выводного отдела правого желудочка локализовано на уровне входа в него. Этот тип характеризуется резкой гипертрофией проксимального отдела конусной перегородки, которая имеет нормальные размеры либо несколько удлинена. 3. Тубулярный тип обструкции, при котором стеноз обусловлен выраженной неравноделенностью конуса. Выводной отдел правого желудочка резко гипоплазирован, сужен и укорочен. Гипертрофия конусной перегородки, как правило, отсутствует. Обычно наблюдаются гипоплазия кольца легочного клапана и стеноз его за счет сращения створок. 4. Многокомпонентное сужение, обусловленное значительным удлиннением конусной перегородки или высоким отхождением модераторного пучка. Существуют 2 основных варианта стеноза: а) с гипертрофией перегородочно-краевой трабекулы и передней папиллярной мышцы двухкамерный правый желудочек); б) с высоким расположением резко гипертрофированного модераторного пучка и одновременно низким внедрением конусной перегородки. Гипертрофия мышцы правого желудочка наблюдается даже у маленьких детей с тетрадой Фалло. Признак этот постоянен является следствием резко повышенной нагрузки на миокард правого желудочка. В комплексе анатомии тетрады Фалло имеются еще 2 особенности. Первая – развитие коллатерального кровообращения в сосудах малого круга, вторая – изменения сосудов легких, которые при данном пороке претерпевают значительную перестройку. Некоторые сосуды склерозируются, облитерируются, в просвете их иногда образуются многоствольные сосуды. Можно наблюдать образование тромбов в системе мелких разветвлений легочной артерии, затем полную окклюзию ряда сосудов легких, а также реканализацию их. Тетрада Фалло может сочетаться с дефектом межпредсердной перегородки (пентада Фалло). Примерно у 2 % больных с тетрадой Фалло имеется открытый артериальный проток. Нередко обнаруживается добавочная левосторонняя верхняя полая вена. Некоторые авторы считают, что тетрада Фалло характеризуется гипоплазией левого желудочка. Этот признак нельзя читать патогномоничным, однако у ряда больных может наблюдаться уменьшение полости левого желудочка. ГемодинамикаВ основе нарушений геодинамики при тетраде Фалло лежит 2 анатомических фактора: стеноз выводного отдела правого желудочка и дефект межжелудочковой перегородки. Для больных тетрадой Фалло характерны уменьшение минутного объема в малом круге кровообращения и сброс венозной крови в аорту. Такой тип гемодинамики встречается приблизительно у 75–80 % больных. Правый желудочек при классической форме порока преодолевает сопротивление стенозированного выходного отдела и сосудистое сопротивление большого круга кровообращения. Величина сброса крови бывает различной, у тяжелобольных она может достигать 70–80 %. Когда стеноз выводного отдела правого желудочка невелик и сопротивление, вызываемое им, меньше сосудистого сопротивления большого круга, возникает артериовенозный сброс крови. Такой тип нарушения гемодинамики лежит в основе так называемой бледной формы тетрады Фалло. У этой категории больных гемодинамика в известной степени аналогична таковой при дефекте межжелудочковой перегородки со стенозом легочной артерии. Клиническая картинаПо существу степень сужения выводного тракта правого желудочка и легочной артерии определяет клиническую картину тетрады Фалло. Различают следующие клинические формы болезни: 1) тяжелая форма с ранним проявлением выраженного цианоза и одышки; 2) классическая форма – цианоз появляется в раннем возрасте, когда ребенок начинает ходить; 3) тяжелая форма, характеризующаяся одышечно-цианотическими приступами; 4) форма болезни с поздним появлением цианоза (в возрасте 6—10 лет), когда окружающие больного начинают замечать появление синевы губ; 5) так называемая бледная форма тетрады Фалло. Такое несколько схематичное выделение различных типов клинического течения болезни оправдано, потому что дает возможность охарактеризовать различные формы проявления этого тяжелейшего порока сердца. У детей с тяжелыми формами тетрады Фалло уже с 3–4 месяцев появляется цианоз губ при крике и плаче. У большинства детей этой группы выявляется стабильный цианоз видимых слизистых и кожных покровов, резко усиливающийся при физической нагрузке или эмоциональном напряжении. Очень тяжело протекает болезнь при развитии одышечно-цианотических приступов, заключающихся в резком усилении цианоза и одышки. Приступы бывают разнообразными по своим клиническим проявлениям. У некоторых больных они кратковременны и не приводят к потере сознания, у других больных они могут привести даже к коматозному состоянию. Описаны случаи смерти или развития тяжелого нарушения мозгового кровообращения, являющиеся следствием одышечно-цианотических приступов. Для тетрады Фалло характерно появление резчайшей слабости, головокружения, тахикардии, усиление цианоза после физической нагрузки. Оценка общего состояния больного тетрадой Фалло представляет определенные трудности. Нередко можно наблюдать больных с выраженным цианозом и достаточной активностью и, наоборот, с едва заметной синевой губ, но вынужденных большую часть времени проводить в постели. Правильное представление о тяжести течения заболевания можно получить, оценивая состояние физической активности больного. Одним из ведущих клинических признаков порока является цианоз видимых слизистых оболочек и кожных покровов. Характер окраски и интенсивность синевы могут быть самыми разнообразными в зависимости от тяжести состояния, развития коллатералей в легких, степени физической нагрузки. У больных со стойким и длительно существующим цианозом отмечается своеобразное утолщение ногтевых фаланг пальцев рук, причем вначале обычно происходит изменение формы ногтей в виде часовых стекол, а затем уже деформируются пальцы, напоминая барабанные палочки. При этом нарушения строения костной основы фаланг не наступает, их утолщение происходит за счет мягких тканей (реакция на длительно существующую гипоксемию и компенсаторную полицитемию). Для тяжелобольных с тетрадой Фалло характерной является вынужденная поза во время отдыха: они часто присаживаются на корточки или лежат с приведенными к животу ногами. С помощью оксиметрических исследований, проведенных у этих больных, установлено, что в таком положении, как правило, повышается насыщение крови кислородом. Вид больных с тетрадой Фалло характерен, они обычно кахектичны, вялы, адинамичны. Однако иногда можно видеть детей с выраженным цианозом, но хорошо развитых. Деформация грудной клетки у больных с тетрадой Фалло крайне редка. При аускультации слева от грудины во II–III межреберье слышен грубый систолический шум. Интенсивность его колеблется в зависимости от степени сужения выводного отдела правого желудочка и легочной артерии. Обычно шум достаточно грубый и занимает всю систолу. II тон над легочной артерией ослаблен. При резко выраженном сужении выводного отдела правого желудочка удается выслушать лишь короткий, сухой, слабой интенсивности систолический шум. На ФКГ обычно регистрируется ромбовидный шум, занимающий всю систолу и заканчивающийся раздвоенным II тоном. Резко выраженный щелчок закрытия аортального (высокоамплитудный аортальный компонент II тона) клапана обусловливает значительное колебание амплитуды II тона, щелчок закрытия легочного клапана (легочный компонент II тона) короткий, малой амплитуды. Примерно у 4–5 % больных с тетрадой Фалло слева между лопатками выслушивается непрерывный дующий систолический шум, обусловленный наличием коллатералей. При тетраде Фалло наблюдается определенная, хотя и не специфическая электрокардиографическая картина. Характерно значительное отклонение электрической оси сердца вправо. Признаки гипертрофии правого желудочка, однако, не сопровождаются резко выраженными признаками перегрузки и дилатации его. Наличие признаков перегрузки левого желудочка заставляет предположить какие-либо дополнительные аномалии. Рентгенологическая картина достаточно характерна: небольшое увеличение размеров сердца со смещением его границ влево с приподнятым левым контуром за счет гипертрофии правого желудочка (форма деревянного башмачка). Легочный рисунок обычно обеднен, и лишь у больных с развитыми коллатералями он достаточно хорошо выражен и может быть даже усилен. В левой передней косой проекции маленький левый желудочек имеет вид «шапочки», расположенной на увеличенных правых отделах. С помощью эхокардиографии при тетраде Фалло можно видеть клапанный и подклапанный легочный стеноз, гипоплазию кольца легочного клапана, легочного ствола и проксимальных отделов легочных артерий. Локация межжелудочковой перегородки позволяет видеть дефект, определить его локализацию и размеры. Удается также определить расширение и смещение аорты вправо, митрально-аортальный фиброзный контакт. При допплер-эхокардиографии в легочном стволе регистрируется турбулентный систолический поток, с помощью допплер-эхокардиографии возможно рассчитать градиент давления между правым желудочком и легочной артерией. В случае функционирующего аорто-легочного анастомоза в легочном стволе регистрируется дополнительный турбулентный диастолический поток. Катетеризация сердца и ангиокардиография являются наиболее информативными методами диагностики тетрады Фалло. По кривой давления, записанной при выведении катетера из легочного ствола в правый желудочек, можно судить о характере легочного стеноза. В случае подклапанного (инфундибулярного) стеноза градиент систолического давления определяется внутри правого желудочка, тогда как систолическое давление в легочном стволе и инфундибулярном отделе правого желудочка одинаковое. При сочетании клапанного и инфундибулярного стеноза наблюдаются два градиента давления: между полостью желудочка и инфундибулярной камерой и между последней и легочным стволом. Характерным гемодинамическим признаком тетрады Фалло является одинаковое систолическое давление в правом желудочке и аорте, куда нередко удается провести катетер через дефект межжелудочковой перегородки. Программа ангиокардиографического исследования больного с тетрадой Фалло включает правую вентрикулографию, легочную артериографию и аортографию. При правой вентрикулографии наблюдается одновременное контрастирование легочной артерии и аорты. Боковая проекция позволяет определить тип и протяженность стеноза инфундибулярного отдела, состояние кольца легочного клапана. Селективная легочная артериография, выполненная в аксиальной проекции, дает возможность получить очень важную для хирурга информацию об анатомии легочного ствола и проксимальных отделов правой и левой легочных артерий. Аортография, которую следует выполнять с помощью антеградно проведенного из правого желудочка катетера, необходима для выявления коллатерального кровоснабжения легких; иногда с ее помощью удается получить информацию о распределении коронарных артерий. При необходимости проводится левая вентрикулография (для определения величины левого желудочка и исключения сопутствующих пороков). ЛечениеРекомендуется хирургическое лечение. Оно может быть паллиативным или радикальным. Паллиативные операции заключаются в наложении аортолегочных анастомозов с целью увеличения легочного кровотока. Радикальная коррекция порока включает устранение легочного стеноза и закрытие дефекта межжелудочковой перегородки. При необходимости выводной отдел правого желудочка и легочный ствол расширяют с помощью заплаты. В случае невозможности устранить легочный стеноз применяется операция Растелли, заключающаяся в соединении правого желудочка и легочной артерии с помощью клапансодержащего синтетического протеза. ТРАНСПОЗИЦИЯ МАГИСТРАЛЬНЫХ СОСУДОВ Полная транспозиция магистральных сосудов (ТМС) является одним из самых распространенных и тяжелых цианотических пороков. Она встречается у 12–20 % всех больных с врожденными пороками сердца, чаще у лиц мужского пола. Анатомия, классификация, гемодинамикаПод транспозицией магистральных сосудов следует понимать порок, при котором аорта отходит от морфологически правого, а легочная артерия – от морфологически левого желудочка. (Это определение является отражением анатомо-гемодинамического подхода и особенно важно в эру хирургического лечения). При полной ТМС отходящая от правого желудочка аорта в большинстве случаев действительно расположена спереди от легочной артерии, однако описаны случаи полной ТМС с положением сосудов (бок о бок и с аортой, расположенной сзади легочной артерии. При этом различают правосторонее (D) и левостороннее (L) положение восходящей аорты. При полной ТМС аорта, отходящая от правого желудочка, несет венозную кровь, которая, пройдя через ткани, по полым венам вновь возвращается в правое предсердие. Соответственно в легочной артерии малом круге кровообращения циркулирует артериальная кровь. Таким образом, большой и малый круги кровообращения разобщены, и жизнь больного возможна только при наличии сообщения между ними. К так называемой простой ТМС относят случаи полной ТМС, сочетающиеся только с межпредсердным сообщением (чаще всего – открытым овальным окном). Полная ТМС часто сочетается с другими пороками сердца: дефектом межжелудочковой перегородки; стенозом легочной артерии, который может быть клапанным, подклапанным и комбинированным; аномалиями положения сердца и т. д. Сброс крови при полной ТМС носит двусторонний характер, причем степень гипоксемии обратно пропорциональна объему сброса. В тех случаях, когда величина сообщения между большим и малым кругами кровообращения недостаточна, развивается компенсаторное увеличение минутного объема сердца, что приводит к его значительной объемной перегрузке и в дальнейшем к развитию сердечной недостаточности. При дефекте межжелудочковой перегородки, ведущем к резкому увеличению легочного кровотока, у больных полной ТМС развивается высокая легочная гипертония. Клиническая картинаОсновной симптом порока – резкий тотальный цианоз, появляющийся с первых дней жизни больного. В остальном в первые две недели жизни клинические признаки порока не проявляются, а затем развивается постепенное увеличение размеров сердца, сопровождающееся признаками декомпенсации. Наблюдаются одышка, тахикардия, отмечаются резкое увеличение печени, отеки, асцит. Обычно имеет место сердечный горб. Выражены симптомы «барабанных палочек», «часовых стекол», полицитемический синдром. При аускультации наблюдается акцент II тона на основании сердца. Шумы могут отсутствовать; выслушиваемый систолический шум, как правило, обусловлен стенозом легочной артерии. ЭКГ характеризуется правограммой и признаками перегрузки и гипертрофии правого желудочка и правого предсердия. Если порок сочетается с дефектом межжелудочковой перегородки, возможны признаки гипертрофии и левого желудочка. Рентгенологическое исследование отражает состояние малого круга кровообращения: признаки гиперволемии и легочной гипертонии свидетельствуют о наличии дефекта межжелудочковой перегородки, обеднение легочного рисунка – о наличии легочного стеноза. Сосудистый пучок в переднезадней проекции узкий, в боковой – расширенный. Характерно нарастающее увеличение размеров сердца, тень которого может иметь яйцевидную форму, хотя встречаются различные варианты ее конфигурации. Двухмерная эхокардиография выявляет прямые признаки порока: параллельное расположение магистральных сосудов и выводных отделов желудочков, отхождение аорты от морфологически правого, а легочной артерии – от морфологически левого желудочка, расположение аорты спереди и обычно справа от легочной артерии, наличие митрально-легочного фиброзного контакта. Локация межпредсердной и межжелудочковой перегородок выявляет их дефекты. Кроме того, можно установить изменения легочного ствола и атриовентрикулярных клапанов. При катетеризации сердца обычно удается провести катетер в левые отделы, в которых насыщение крови кислородом достаточно высокое. Повышение систолического давления в левом желудочке при полной ТМС говорит о наличии дефекта межжелудочковой перегородки или стеноза легочной артерии. Поэтому, когда речь идет об оперативном лечении порока, особенно важно провести катетер в легочную артерию, что при полной ТМС связано с определенными трудностями. При ангиокардиографическом исследовании контрастное вещество вводят в правый желудочек и левые отделы сердца. Это позволяет выявить отхождение аорты от правого, а легочной артерии от левого желудочка, расположение аорты, как правило, спереди от легочной артерии, межжелудочковое сообщение. Ангиокардиографическая диагностика легочного стеноза при полной ТМС представляет значительные трудности, методом выбора для диагностики его служит левая вентрикулография в проекции «длинной оси сердца». Для исключения открытого артериального протока производится аортография. ЛечениеСуществует много паллиативных и радикальных способов оперативного лечения полной ТМС. Для спасения жизни новорожденных, находящихся в критическом состоянии, применяют баллонную атриосептостомию, заключающуюся в разрыве межпредсердной перегородки при катетеризации сердца с помощью баллончика. Применяются также паллиативные операции: 1) иссечение межпредсердной перегородки; 2) различные виды системно-легочных анастомозов при легочном стенозе; 3) сужение легочной артерии при легочной гипертонии. К радикальным операциям относится прежде всего внутрипредсердная коррекция порока. Операция заключается в подшивании заплаты внутри правого предсердия таким образом, чтобы направить кровоток из полых вен через митральный клапан в левый желудочек, от которого отходит легочная артерия. При этом кровь из легочных вен через трикуспидальный клапан попадает в правый желудочек, от которого отходит аорта. Осложнениями данных операций являются повреждение проводящих путей сердца и обструкция полых и легочных вен. При определенном положении и большой величине дефекта межжелудочковой перегородки имеется возможность создать тоннель между левым желудочком и аортой с помощью синтетической заплаты, сохранив сообщение легочной артерии с правым желудочком через дефект, т. е. осуществить внутрижелудочковую коррекцию полной ТМС. Однако большее распространение получила операция при которой артериальная кровь через дефект межжелудочковой перегородки с помощью заплаты направляется в аорту, выход из левого желудочка в легочную артерию закрывается, а из правого желудочка посредством синтетического протеза в нее направляется венозная кровь. В Институте сердечно-сосудистой хирургии им. А. Н. Бакулева РАМН детям первых 3 лет жизни выполняются операции внутрипредсердной коррекции порока по методу Мастарда и Сеннинга, а у детей более старшего возраста при наличии дефекта межпредсердной перегородки и легочного стеноза предпочтение отдается операции Растелли. |
|
|||
|
Главная | В избранное | Наш E-MAIL | Добавить материал | Нашёл ошибку | Наверх |
||||
|
|
||||
